طیف جذبی طیف نشری
طیف جذبی :
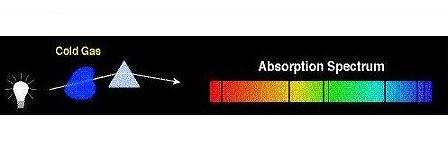
وقتی به یک ماده نوری را میتابانیم ماده قسمتی از نور تابیده شده را جذب کرده
وباقی را عبور دهد اگر نور عبور کرده را از یک منشور عبور دهیم به طیف حاصله
طیف جذبی میگویند . طیف جذبی میتواند خطی یا پیوسته باشد
طیف نشری :
اگر یک ماده را از طریق حرارت دادن ویا قوس الکتریکی و یا یه هر طریق دیگر به
شدت گرم کنیم ماده از خود نور تابش میکند ( پدیده نشر ) در صورتیکه تابش
نشرشده را از یک منشور عبور دهیم به طیف حاصله طیف نشری گفته میشود
طیف نشری هم میتواند خطی یا پیوسته باشد

طیف نشری خطی
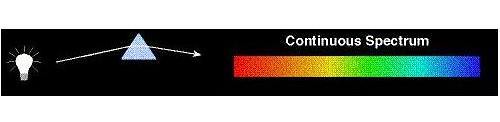
طیف نشری پیوسته
طیف نشری خطی اتم ها :
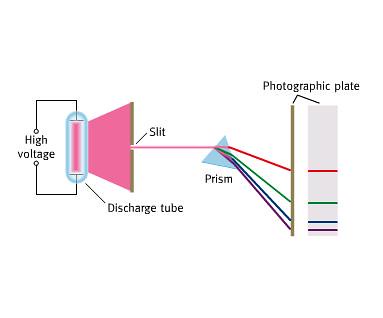
اگر اتم های گازی شکل یک عنصر را در یک قوس الکتریکی ، یک جرقه الکتریکی ،
ویا شعله گرم کنیم نور از آنها منتشر میشود . اگر شعاعی از این نور را توسط
منشور تجزیه کنیم یک طیف خطی حاصل میشود از این رو به آن طیف نشری
خطی اتمی میگویند
برای بررسی چگونگی این پدیده ، اتم هیدروژن را در نظر میگیریم :
اتم هیدروژن تنها دارای یک الکترون است واین الکترون در پایین ترین مدار آن
یعنی مدار اول قرار داردبه این حالت، حالت پایه می گویند . وقتی اتم هیدروزن
را گرم کنیم الکترون آن تحریک شده وبا جذب انرژی از تراز پایه به تراز های بالاتر
می جهد این حالت را حالت برانگیخته می گویند . ولی الکترون در تراز های بالا
ناپایدار بوده و با رها کردن انرژی جذب کرده به تراز های پایین تر بر می گردد و این
بار انرژی کسب کرده را به صورت تابش بر می گرداند
اگر الکترون از تراز i به تراز f ارتقا یابد به اندازه تفاوت انرژی این دو تراز یعنی
به اندازه( Ef – Ei) انرژی جذب میکند و در برگشت در صورتی که به همان تراز i
برگردد همان مقدار انرژی را نشر میکند .
بنابراین می توان نتیجه گرفت هرچه تفاوت انرژی دو لایه بیشتر باشد انرژی نور
نشری بیشتر و طول موج آن کوتاه تر است . طول موج تابش نشر شره در
انتقالات را می توان با بکار گیری فرمول زیر محاسبه کرد
در شکل زیر کلیه انتقالات الکترونی اتم هیدروژن نشان داده شده اند
چنانچه روشن است در انتقالات اتم هیدروزن چندین سری دیده میشود :
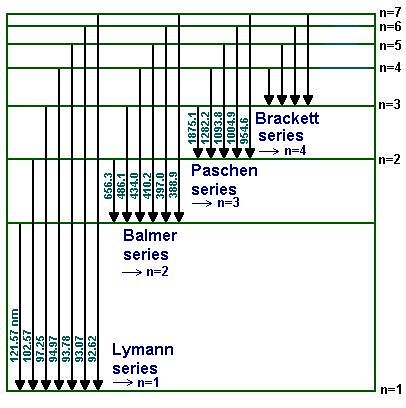
ا) سری لیمان : ( ni→n1 ) چون در این انتقالات برگشت به تراز اول صورت
میگیرد . انرژی نور حاصله بسیار بالا بوده و طول موج ان به قدری کوتاه است که
در منطفه فرا بنفش قرار می گیرد . از این رو سری لیمان طیف قابل دیدن ندارد
2) سری بالمر ( ni→n2 ) : در این سری ، الکترون برانگیخته به تراز دوم بر
میگردد . انرژی وطول موج مربوط به این انتقالات در محدوده مرئی بوده و طیف آن
قابل دیدن است
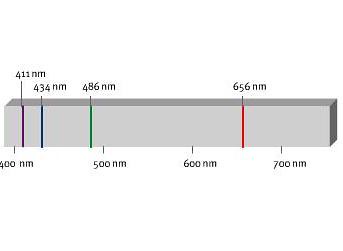
4 طیف مرئی در سری بالمر ناشی از انتقالات زیر هستند :
( n6→n2 ) به رنگ بنفش با طول موج ۴۱۰ نانومتر
( n5→n2 ) به رنگ آبی با طول موج ۴34 نانومتر
( n4→n2 ) به رنگ سبزبا طول موج 486 نانومتر
( n3→n2 ) به رنگ قرمز با طول موج۶۵۶ نانومتر
برای دستیابی به انیمیشن چگونگی تابش اتم ئیدروژن و خطوط طیفی آن برروی
لینک کلیک کنید
3) سری پاشن ( ni→n3 ) : بر گشت الکترون به تراز سوم میابشد . اختلاف
انرژی در تراز های بالاتر کمتراست بنابراین در سری پاشن اختلاف انرژی به قدر
کافی کم وطول موج به اندازه کافی بزرگ است که این انتقالات در محدوده
فروسرخ قرار بگیرند از این روطیف سری پاشن هم قابل رویت نیست
4) سری براکت ( ni→n4 ): برگشت به تراز چهارم است و مانند سری
لیمان در محدوده فروسرخ قرار گرفته از این رو سری براکت نیز طیف مرئی
ندارد
نکته
1. هم در طيف نشری و هم در طيف جذبي هر عنصر ، طول موجهاي معيني
وجود دارد كه از ويژگيهاي مشخصه آن عنصر است. يعني طيفهاي نشری و
جذبي هيچ دو عنصري مثل هم نيست.
2. اتم هر عنصر دقيقا همان طول موجهايي از نور سفيد را جذب ميكند كه اگر
دماي آن به اندازه كافي بالا رود و يا به هر صورت ديگر بر انگيخته شود، آنها را تابش ميكند.
http://chem1234.blogfa.com/post-204.aspx
 با سلام به تمام دانش آموزان و تلاشگران عرصه آموزش و يادگيري .
با سلام به تمام دانش آموزان و تلاشگران عرصه آموزش و يادگيري .